Доктор. Дональд Кон занимается разработкой генной терапии редких детских иммунных нарушений более 30 лет. На этой неделе его роль в клиническом исследовании достигла кульминации в первом в истории одобренном Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США лечении тяжелого дефицита адгезии лейкоцитов I — генетического состояния, характеризующегося рецидивирующими инфекциями и, зачастую, ранней смертью.
Редким педиатрическим заболеванием страдает примерно один из миллиона детей во всем мире. Мутации в гене ITGB2 нарушают нормальную функцию двух белков — CD11 и CD18, которые работают вместе, помогая лейкоцитам достигать инфекций и реагировать на них. Когда этот процесс нарушается, дети становятся восприимчивыми к рецидивирующим, опасным для жизни бактериальным и грибковым инфекциям. Без лечения выживание после детского возраста редко.
Одобрение терапии, продаваемой под названием Креслади, было основано на результатах клинического исследования, проведенного в Калифорнийском университете в Лос-Анджелесе Коном, членом Центра регенеративной медицины и исследований стволовых клеток Эли и Эдит Броуд.
Ежегодно видеть этих пациентов во время последующих посещений и видеть, что они больше не борются с опасными для жизни инфекциями, было невероятно
Исследователи набрали девять пациентов в возрасте от 5 месяцев до 9 лет с тяжелой формой LAD-I со всего мира. Небольшая когорта отражает редкость этого заболевания. Из девяти пациентов команда Калифорнийского университета в Лос-Анджелесе включила и вылечила шестерых; троих лечили в Лондоне и Испании.
Клиническое исследование проводилось в сотрудничестве между исследователями Калифорнийского университета в Лос-Анджелесе и компанией Rocket Pharmaceuticals, которая спонсировала исследование.
Генная терапия с использованием собственных клеток пациентов
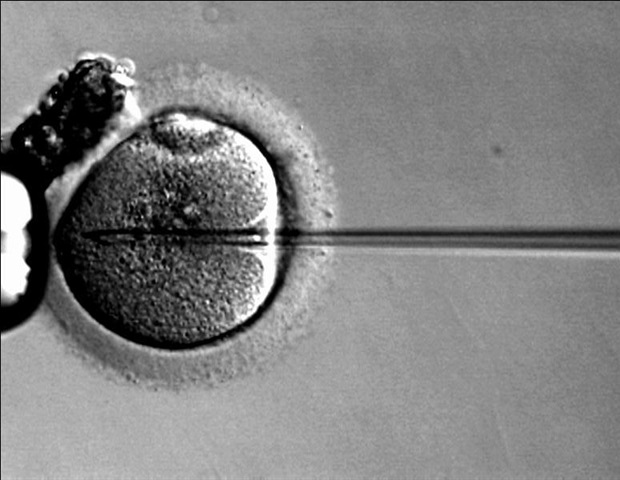
Однократная генная терапия заключается в добавлении здоровой копии гена ITGB2 в стволовые клетки крови каждого ребенка, а затем возвращении этих клеток этому ребенку, что позволяет его организму вырабатывать функциональные иммунные клетки для борьбы с инфекциями и более быстрого заживления ран. Используя собственные клетки пациентов, терапия позволяет избежать риска отторжения иммунной системы, связанного с донорскими клетками, или реакции «трансплантат против хозяина».
Мы обнаружили что для пациентов, которых мы лечили, эта терапия связана с меньшим количеством краткосрочных и долгосрочных токсичностей, чем те, которые часто связаны с трансплантацией костного мозга, которая требует гораздо большего количества химиотерапии и иммунодепрессантов до и после трансплантации".
Д-р. Дональд Кон, член Центра регенеративной медицины и исследований стволовых клеток Эли и Эдит Броуд
Все девять пациентов, участвовавших в исследовании, выжили, не нуждаясь в трансплантации костного мозга, и не было зарегистрировано ни одного случая отказа трансплантата или иммунного отторжения. Важно отметить, что данные показали значительное снижение числа тяжелых инфекций, требующих пребывания в больнице.
У детей до начала лечения высокое количество лейкоцитов, или лейкоцитоз, постоянно улучшалось, и исследователи наблюдали устойчивое присутствие терапевтического гена и увеличение экспрессии CD18 и CD11a, что имеет решающее значение для функционирования иммунной системы.
От десятилетий исследований до одобрения FDA
Эта новость знаменует собой важную веху для Кон, который более трех десятилетий потратил на разработку и тестирование генной терапии иммунных заболеваний. Креслади станет первым из этих методов лечения, в разработке которого принимал участие Кон, получившим одобрение FDA - важный шаг в обеспечении того, чтобы терапия могла достичь пациентов, которые в ней нуждаются.
Ожидается, что разработанная Rocket Pharmaceuticals терапия станет доступной через специализированные лечебные центры, имеющие опыт проведения процедур генной терапии ex vivo. Подтверждение клинической пользы будет основано на оценке данных долгосрочного наблюдения за пролеченными пациентами в ходе клинического исследования и постмаркетингового реестра.
Это одобрение также является значительной победой для Калифорнийского института регенеративной медицины (CIRM), агентства штата Калифорния, которое финансирует исследования стволовых клеток и генной терапии. Основанная в 2004 году для ускорения терапии стволовыми клетками, CIRM совместно с Rocket финансировала клинические испытания генной терапии и сейчас празднует первое в истории одобрение FDA, ставшее возможным благодаря его поддержке.
Кон надеется, что это одобрение побудит больше компаний разрабатывать методы лечения других редких заболеваний. Он проводит клинические испытания, чтобы проверить лечение другого смертельного заболевания иммунной системы, известного как ADA-SCID, или тяжелого комбинированного иммунодефицита с дефицитом аденозиндезаминазы. Результаты также обнадеживают: данные долгосрочного наблюдения, опубликованные в NEJM в октябре 2025 года, показали 95 % успеха у 62 пролеченных детей без каких-либо серьезных осложнений.
"Надеемся, такое одобрение будет стимулировать другие компании инвестировать в такого рода методы лечения и признать, что существует способ сделать их коммерчески доступными", — сказал Кон.

 01:00
01:00